1型糖尿病治療長期面臨兩難:胰島素雖能保命,卻難阻血糖波動,過量使用引發的嚴重低血糖可致神經損傷甚至死亡。臨床研究證實,干細胞來源的胰島移植物可使糖尿病患者恢復胰島功能,但免疫抑制方案如何優化,始終懸而未決。既往自體研究均局限于因器官移植而需免疫抑制劑的患者,真正的“純凈”自體移植從未實現。

領跑全球!國內實現干細胞胰島移植新突破:1型糖尿病治愈邁出關鍵一步
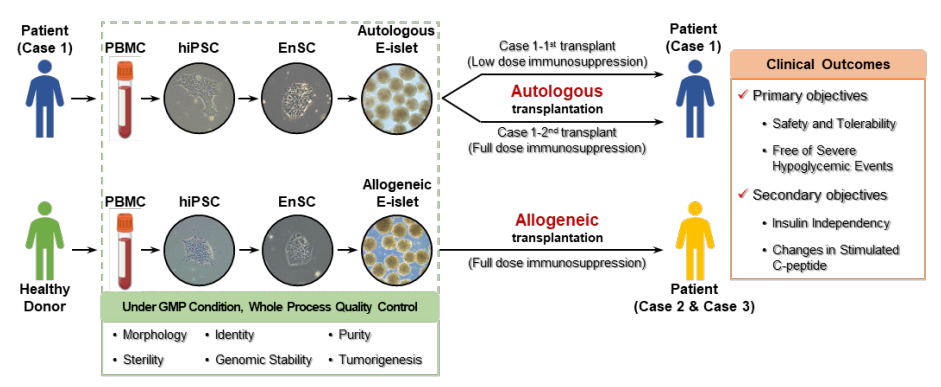
這一困境迎來轉機。近期,中國科學院分子細胞科學卓越創新中心(生物化學與細胞生物學研究所)程新研究組聯合海軍軍醫大學第二附屬醫院(上海長征醫院)殷浩教授團隊在國際學術期刊《柳葉刀·糖尿病和內分泌學雜志》上發表了一篇“針對3例1型糖尿病且移植前內源性胰島β細胞功能完全喪失的受者,采用自體及異體干細胞來源的胰島治療”的研究綜述[1]。

本文報告了三例1型糖尿病合并嚴重低血糖癥患者的治療結果,這些患者接受了自體或異體內胚層干細胞衍生的胰島樣組織(E-胰島),并接受了不同程度的免疫抑制治療。結果表明:成功實現了1型糖尿病患者的胰島功能重建與血糖自主調控。
患者1:自體E-胰島移植后因免疫抑制方案不當及自行停藥導致移植物功能喪失
該患者為30歲女性,1型糖尿病病史長達18年,入組時病情極為復雜且控制極差。盡管自述接受強化管理,但其糖化血紅蛋白(HbA1c)仍達7.6%(60 mmol/mol),基線血糖達標時間(TIR;3.9–10.0mmol/L)為55%(圖1),更重要的是,其嚴重低血糖事件(SHE)發生頻率高達每周4.6次,且伴有低血糖感知受損(Clarke評分5分,提示風險極高)。實驗室檢查證實其胰島功能已完全衰竭,空腹及餐后C肽均低于檢測下限(<0.01nmol/L)。
首次移植采用不含強效免疫抑制劑(他克莫司)的方案,3個月后血糖無改善,提示植入失敗。
第二次輸注后,血糖控制得到顯著改善,表現為目標胰島素抵抗指數(TIR)從術前的48%大幅提高至第23周的97%,糖化血紅蛋白(HbA1c)從基線的8%(64mmol/mol)下降至第23周的6.8%(51mmol/mol)。到第23周時,患者的空腹C肽濃度達到0.33nmol/L(正常范圍0.37–1.47nmol/L),胰島素需求量顯著下降。
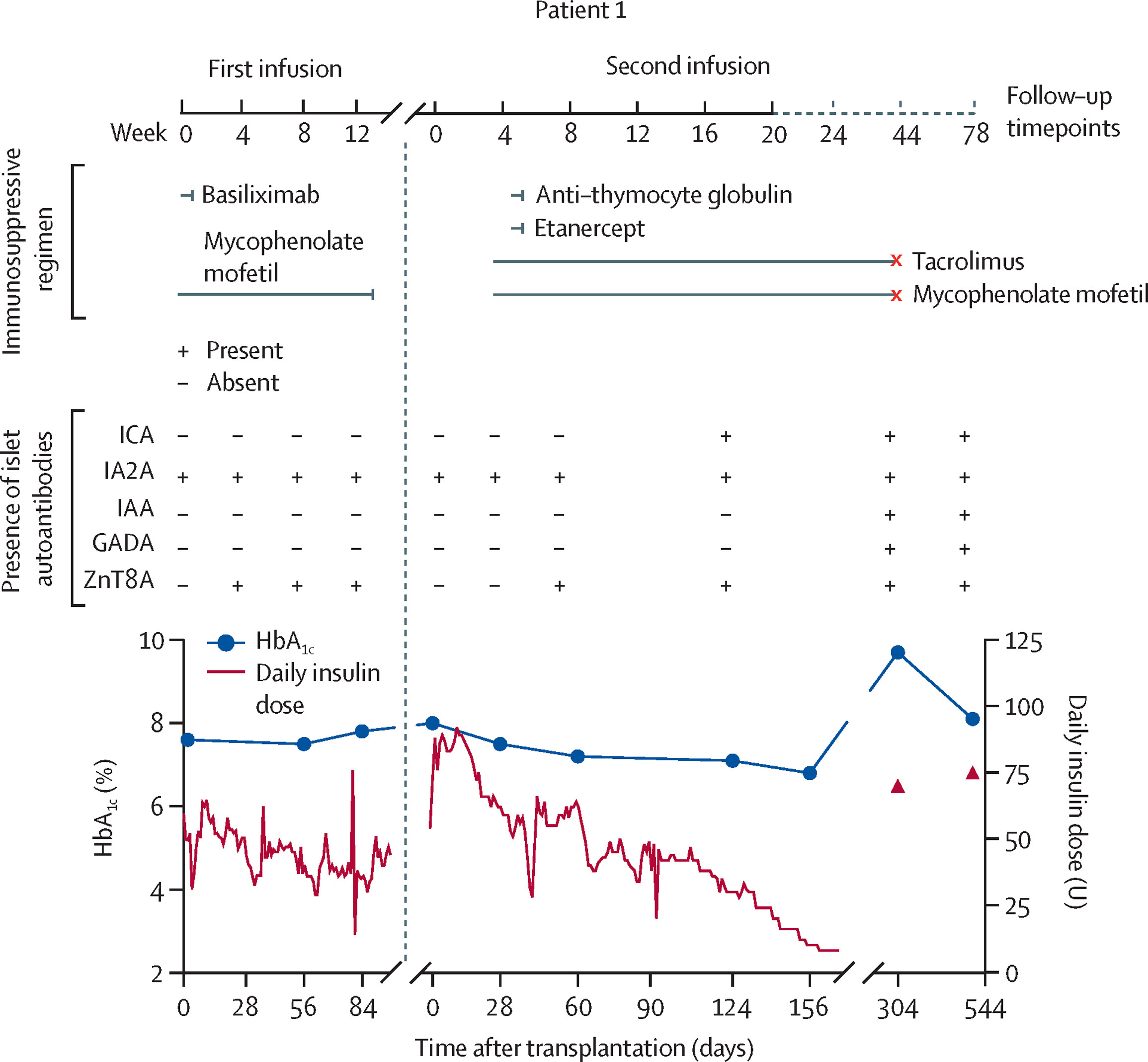
不幸的是,患者因雙相情感障礙加重自行停用免疫抑制藥物,導致移植物被自身免疫系統攻擊而丟失。第44周時HbA1c反彈至9.7%,C肽再次檢測不到,第78周胰島素需求恢復至每日75單位。自身抗體譜變化(ZnT8A反復出現、最終所有抗體陽性)提示自身免疫復發。
患者2:同種異體E-胰島移植后實現完全胰島素獨立和血糖正常
該患者為45歲男性,急性起病糖尿病,入組時頻繁嚴重低血糖(每周4-5次),低血糖感知受損,C肽檢測不到。
接受HLA完全不匹配的同種異體E-胰島移植后,在全劑量免疫抑制保護下,血糖控制實現質的飛躍:TIR從基線時的71%提高到第36周及之后的100%;第5周未發生嚴重低血糖事件;第20周停止發生低血糖事件;HbA1c從基線時的7.2% (56mmol/mol) 下降到第4周的5.7% (39mmol/mol) 和第78周的5.7%;血糖波動性穩定;混合餐耐量試驗顯示胰島素和C肽分泌逐漸恢復;以及第36周完全擺脫胰島素依賴。
最關鍵的是,患者于第36周實現完全不依賴外源性胰島素,混合餐耐量試驗證實胰島功能完全恢復。至最后一次隨訪,已維持該狀態26個月。
患者3:同種異體E-胰島移植后血糖顯著改善但仍有部分胰島素需求
患者3為15歲女性,青少年起病的1型糖尿病,GADA抗體陽性。其病情特點在于極度的血糖波動和不良的自我管理。入組前,因飲食不當導致胰島素濫用(>80 U/天),雖經規范內分泌管理后胰島素劑量下調至56.5U/天并聯合二甲雙胍,但血糖控制依然極差:HbA1c高達8.7%,TIR僅25%,同時伴有復發性嚴重低血糖(每周1-2次)和酮癥酸中毒。C肽同樣檢測不到。
移植方案與過程(2024年9月2日):患者接受了與患者2相同的全劑量免疫抑制方案,輸注了來自健康供體的、HLA部分不匹配的同種異體E-胰島,劑量為160萬胰島當量(三例中最高)。截至最后一次隨訪,已觀察18個月。
血糖控制的顯著改善:
- TIR:從基線的25%實現了跨越式提升,至第52周達到94%,雖然未及患者2的100%,但已是質的飛躍。
- 低血糖事件:在第42周之后,低血糖事件完全消除,解決了青少年患者最危險的問題之一。
- HbA1c:從基線8.7%穩步下降至第52周的6.7%,雖未完全正常,但已接近理想控制目標。
胰島功能部分恢復與外源性胰島素需求:
- C肽分泌:混合餐耐量試驗證實移植物功能恢復。第52周時,空腹C肽為0.51nmol/L(已進入正常范圍),餐后峰值可達1.07 nmol/L,顯示了良好的胰島儲備功能。
- 胰島素劑量:外源性胰島素需求量從基線的56.5U/天大幅減少至第52周的16U/天,并僅需間歇口服二甲雙胍。這表明移植的胰島細胞承擔了大部分機體所需的胰島素分泌工作,但尚未能完全替代。
小結:患者3是另一例成功的同種異體移植案例。它同樣實現了血糖控制的革命性改善,消除了嚴重并發癥。但與患者2達到“完全”胰島素獨立不同,本例患者在18個月的隨訪時點仍需少量外源性胰島素輔助。
這背后的原因可能是多方面的,包括患者年齡、疾病特征、移植胰島劑量的差異(患者2為60萬,患者3為160萬,劑量與效果并非簡單線性關系)、HLA匹配程度的不同,或個體對免疫抑制藥物的反應差異等。盡管如此,該結果依然極具臨床價值,它標志著即使是病情復雜、控制極差的青少年患者,也能從E-胰島移植中獲益,大幅改善生活質量并減少并發癥風險。
免疫抑制:干細胞療法光環下的“達摩克利斯之劍”
過去五年臨床試驗反復印證:無論自體抑或異體干細胞衍生胰島移植,均具良好耐受性,可助患者擺脫胰島素依賴。然而,成功的鐵律是——免疫抑制不可缺位。本研究首次以沉痛教訓證實,即便自體移植物,若免疫抑制不足,自身免疫攻擊仍可卷土重來。低劑量誘導方案遠不足以筑起防線。
理論上自體移植可豁免長期免疫抑制,但臨床現實卻是:所有接受干細胞衍生胰島治療的患者,皆需維持性免疫抑制。這道防線同時帶來惡性腫瘤與感染風險,對兒童及無嚴重并發癥者尤甚。未來或可探索“溫和免疫抑制”方案,但現有證據表明,僅憑抗體水平難測療效。需開發更精準的評估工具,如體外T細胞反應檢測,方能為個體化減量用藥鋪路。
研究同時指明未來方向:厘清影響移植物存續的關鍵因素,區分自身免疫復發與同種異體排斥。長期追蹤T細胞動態,結合HLA分型與移植物存活數據,有望優化供受者配型策略。此外,青春期胰島素抵抗等因素亦需納入考量——移植物存活不等于胰島素獨立,綜合管理方為制勝之道。
三例患者,三種結局,勾勒出干細胞治療糖尿病的清晰圖景:技術可行,免疫為限。這條路,曙光已現,征途猶長。
參考資料:[1]Shi Y, Feng Y, Li T et al.Autologous and allogeneic stem cell-derived islet therapy in three recipients with type 1 diabetes and complete loss of endogenous pancreatic β-cell function pretransplantThe Lancet Diabetes & Endocrinology, 2026; 14, 285-288
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信